中国排球超级联赛保定第一阶段赛程安排一览
2023-10-30
更新时间:2023-10-02 20:08:37作者:无忧百科

参考文献:
10.2
知识分子
The Intellectual

导 读
刚刚,2023年诺贝尔生理学或医学奖宣布授予德国生物技术公司BioNTech的卡塔琳·卡里科(Katalin Karikó)、美国宾夕法尼亚大学教授德鲁·魏斯曼(Drew Weissman),以表彰他们在核苷碱基修饰方面的发现,这些发现使得针对 COVID-19 的有效 mRNA 疫苗得以开发。
两位科学家的突破研究使得高效率的新冠mRNA疫苗得以被快速研发,也已凭此获得了多项大奖,包括2022年美国科学突破奖(Breakthrough Prize)、2021年拉斯克基础医学研究奖(The Lasker Awards)、2023年盖尔德纳奖等。
迄今为止,共有225名科学家获得过诺贝尔生理学或医学奖(截至2022年颁完奖),刚刚得奖的卡塔琳·卡里科是第13位获得该奖的女性科学家。
在卡塔琳·卡里科之前,得过该奖的女性科学家包括格蒂·科里(1947年)、罗莎琳·萨斯曼·耶洛(1977年)、巴巴拉·麦克林托克(1983年)、丽塔·列维-蒙塔尔奇尼(1986年)、格特鲁德·B·埃利恩(1988年)、克里斯汀·纽斯林-沃尔哈德(1995年)、琳达·巴克(2004年)、弗朗索瓦丝·巴尔-西诺西(2008年)、伊丽莎白·布莱克本(2009年)、卡罗尔·格雷德(2009年)、迈-布里特·莫泽(2014年)和屠呦呦(2015年)。
撰文 |郭晓强 叶水送 闫思宇
责编 |刘楚 叶水送

卡塔琳·卡里科(Katalin Karikó)

德鲁·魏斯曼(Drew Weissman)

新冠疫情以来,辉瑞-BioNTech和Moderna的mRNA疫苗获得广泛应用,这种疫苗递送的mRNA能指导细胞制造新冠病毒刺突蛋白,从而引发人体抗体表现。但曾有几十年的时间里,mRNA疫苗被认为是不可行的,因为注射mRNA会诱发不必要的免疫反应,导致mRNA被即刻降解。

图1卡塔琳·卡里科(Katalin Karikó)和德鲁·魏斯曼(Drew Weissman)
而卡塔琳·卡里科和德鲁·魏斯曼在2005年前后发现,将mRNA中一种称为尿苷(uridine)的分子替换成类似的分子假尿苷(pseudouridine),就能避免这种免疫反应的发生。
2020年4月,作为被寄予厚望、结束新冠大流行的关键工具,《纽约时报》发表长文介绍mRNA疫苗以及技术背后的卡里科,65岁的卡里科才被公众广泛了解。
这一年里,mRNA技术几乎获得了所有重量级的科学大奖,然而在之前的学术研究生涯里,卡里科本人始终未能获得终身教职,并在后期选择加入德国生物技术公司BioNTech从而步入工业界。
另一位同样不可忽视的mRNA技术重要贡献者,就是卡里科在宾夕法尼亚大学时的同事、免疫学家德鲁·魏斯曼。两人相识于1997年,魏斯曼刚刚成为宾夕法尼亚大学的一名新教员之后,二人在使用学校中的复印机时偶遇,等待中攀谈起来并互相介绍自己的工作,促成了今后的合作。
mRNA与疫苗
1953年,DNA双螺旋模型的提出,在证明DNA是遗传信息携带者的同时也确立了DNA的重要地位。1958年,克里克提出“中心法则”,详细阐明了遗传信息流动方向: 首先以DNA为模板,通过转录产生RNA;再以mRNA为模板,通过翻译产生蛋白质,而蛋白质是生物学功能的直接执行者。
1961年,研究人员正式发现mRNA,从而开启对这种生物大分子的系统研究。不久,研究人员破译了mRNA遗传密码,从而在mRNA与蛋白质之间建立了线性关系,即知道mRNA序列就可确定蛋白质的信息,而知道蛋白质序列在一定程度上也可以推测mRNA信息。这一发现极大推动了mRNA的发展和应用。
应用mRNA的想法可追溯到20世纪70年代末,但到90年代才开始研究。科研人员直接为动物注射mRNA后发现,这些mRNA可产生活性蛋白质,发挥特定生物学功能,这意味着 传统使用蛋白质可以实现的目标,mRNA也可以完成。
但将mRNA应用于疫苗的尝试遇到许多挑战。合格疫苗需满足两个基本条件:首先是安全性,由于疫苗是为健康人所用,故对安全性要求极为严格;其次是有效性,只有达到一定保护率才能真正遏制疾病的传播。而mRNA作为疫苗在这两方面都有问题。
首先,将mRNA直接注射到实验动物体内可引发强烈的非特异性免疫反应,严重造成死亡;其次 ,mRNA稳定性差(对保存条件要求较为严格),在体内表达效率低(无法产生足量蛋白质),无法真正激发抗病毒能力。因此科学界和制药界对mRNA应用前景并不看好,许多研究人员在经过尝试后纷纷放弃。
但当时作为生物化学家的卡里科坚持了下来,她最终与魏斯曼合作解决了mRNA疫苗应用过程中的诸多问题。比如:通过对体外合成的mRNA进行碱基修饰而大大减弱免疫原性,从而减少非特异毒性反应发生;通过去除mRNA混杂的双链RNA而进一步降低毒性,同时提高蛋白质翻译效率,使特异性免疫应答增加。
但正如卡里科在接受采访时感叹道,“现在每个人都明白mRNA技术的重要性,可惜那时候却没有。”
从匈牙利到美国
1955年,卡里科出生于匈牙利东部小镇小新萨拉什,从小就对自然科学感兴趣。1972年,卡里科进入匈牙利最著名的大学之一塞格德大学就读,并于1977年遇见了自己未来的丈夫贝拉·弗朗西亚(Béla Francia)。1978年,卡里科在塞格德大学拿到了博士学位,随后进入塞格德生物研究中心工作,主要研究RNA。
1985年,塞格德生物研究中心因缺少经费开始减员,卡里科被裁后申请到了美国天普大学的博士后职位,便离开了匈牙利。
1989年,她以助理研究员的身份从天普大学来到宾夕法尼亚大学医学院埃利奥特·巴纳森(Elliot Barnathan)实验室。当时她与巴纳森一起尝试将mRNA注射到细胞中,看是否能产生蛋白质,然后利用同位素技术看这些蛋白质在细胞中哪个位置以及如何发挥作用。然而当时RNA技术不被外界接受,后来巴纳森离开学术界去了一家制药公司,卡里科失去了依靠,就此彻底地失去了研究经费来源。
1997年是卡里科研究生涯的重要转折点,她在宾夕法尼亚大学医学院偶然碰见刚加入医学院的新教员魏斯曼。魏斯曼向她介绍自己是研究艾滋病病毒疫苗的,而卡里科则介绍说,“我是一个RNA科学家,可以做有关mRNA的任何事”。
当时魏斯曼一心想研制出艾滋病疫苗,他觉得也许可以试试卡里科的mRNA技术,就这样魏斯曼将卡里科引入到自己的实验室。
1959年8月31日,魏斯曼出生于美国马萨诸塞州列克星敦(Lexington),儿时就显现出较好的科学天赋,最喜欢的事情就是拆解,超强动手能力也促使魏斯曼更倾向于自然科学的学习。
1981年,魏斯曼从布兰迪斯大学(Brandeis University)毕业,获得学士和硕士学位,专业为生物化学/酶学。随后进入波士顿大学医学院,最终于1987年获得医学学位和免疫学/微生物博士学位,魏斯曼在贝斯以色列女执事医疗中心(Beth Israel Deaconess Medical Center, BIDMC)完成住院医师培训。
1989年,魏斯曼放弃了成为一名医生而选择加入美国国立卫生研究院福奇(Anthony Fauci)实验室从事博士后研究,重点是传染性疾病。
1997年,38岁的魏斯曼加入宾夕法尼亚大学,正式开启自己独立的职业生涯,结识了科研挚友卡里科。
完美的合作
魏斯曼和卡里科合作是一个非常成功的典范,源于两个原因,首先知识互补,其次是幸运的选择。疫苗是mRNA最佳应用方向,尽管mRNA提供无限可能,而疫苗无疑是最成功的,如果不是疫苗而是药物的话,可能还要等上几年甚至几十年。
此外,他们合作的时机也刚刚好。1996年,科学家发现固有免疫作用机制,这为避免mRNA免疫反应提供必要的理论支持,意味着如果他们合作时间提前,将很难解决mRNA应用难题,而太晚别人就可能捷足先登。
尽管合作计划达成,但真正实施起来仍是困难重重,消除炎症反应当仁不让成为解决mRNA疫苗开发的重中之重。卡里科更多负责mRNA改进,而魏斯曼则负责免疫性检测。
先补充一点基础知识。免疫系统具有识别 “自我” 和 “非我” 的能力,而体外合成的mRNA可被固有免疫系统作为“非我”的外界入侵物对待将其破坏,因此无法到达细胞内发挥作用。mRNA是一种由4种核苷酸按照不同排列顺序形成的单链结构,四种核苷酸差别在于碱基不同,分别对应腺嘌呤(A)、鸟嘌呤(G)、胞嘧啶(C)和尿嘧啶(U)。魏斯曼和克里克研究的向就转化为如何能操作RNA以逃过免疫系统的监视。
结果几年试错和改进完善,二人终于在2005年发现mRNA引发免疫应答的问题所在,那就是尿嘧啶(U)惹的祸,它与核糖有两种连接方式,正常情况下形成尿苷(下图左),但特殊情况下还形成假尿苷(Ψ)(下图右),恰恰就是这个微小差别则产生不同后果。魏斯曼和克里克发现使用Ψ代替U后形成的修饰mRNA,可有效躲避免疫系统的识别而不再出现炎症反应。

图2天然mRNA(左)和修饰mRNA(右)
这一发明在著名的《Immunity》杂志发表,同时申请专利,对推动mRNA应用具有里程碑意义。
mRNA疫苗的应用和研发
2005年,斯坦福大学读博士后德约克·罗西(Derrick Rossi)注意到了卡里科和魏斯曼发表在《Immunity》上的论文,他认为这篇文章很有开创性,当时他主要从事干细胞方面研究,希望通过这种修饰后的mRNA来让成熟的细胞重编程,重新回到干细胞的状态。
2009年,罗西的研究颇有进展,于是他告诉哈佛医学院的蒂莫西·斯普里格(Timothy Springer)这一结果,斯普里格同时是一位医药企业家。随后,斯普里格告诉了更资深的学者罗伯特·兰格(Robert Langer),兰格建议罗西可以用 “这个技术来研发药物、疫苗,以及其他所有的可能”。
2010年,罗西、兰格、斯普里格以及 Kenneth Chien,一起成立了莫德纳(Moderna)公司。2014年,罗西从莫德纳公司退休,目前他在莫德纳公司没有任何职务。
而在2006年,卡里科和魏斯曼也创立了一家公司RNARx,卡里科担任这家公司的CEO,此后RNARx获得了来自政府的90万美元的资助。然而,2010年,宾夕法尼亚大学将卡里科和魏斯曼的专利卖给了实验室供应商Cellscript的老板Gary Dahl。RNARx公司尚未进入临床的项目就此夭折了。
此后,莫德纳的投资公司之一 Flagship Pioneering 曾找到卡里科,只可惜当时这个专利已经被卖掉了。没有专利授权,莫德纳公司只好自己来修饰核酸,并能重复卡里科的结果,2014年,莫德纳获得了自己的专利。与此同时,Gary Dahl 也将卡里科和魏斯曼的核心专利转让给了莫德纳公司和BioNTech公司。
2013年,宾夕法尼亚大学不再续聘卡里科,于是她顺势加入了BioNTech公司担任副总裁,当时BioNTech是一家连自己网站还没有的小公司。
进入公司后,卡里科继续她的研究,以改进mRNA 技术。如保护mRNA分子,使其能保存更长时间,因为mRNA很不稳定,通常情况下需要超低温下才能保存下来。2015 年,卡里科发现用脂质纳米颗粒包裹它们,可防止它们过快降解并促进它们进入细胞。
此后mRNA真的开始在人体进行试验,有7-8个mRNA疫苗的试验项目在开展,但没有一个mRNA疫苗成功获批上市,人们不太相信这个技术能发挥很大的价值。
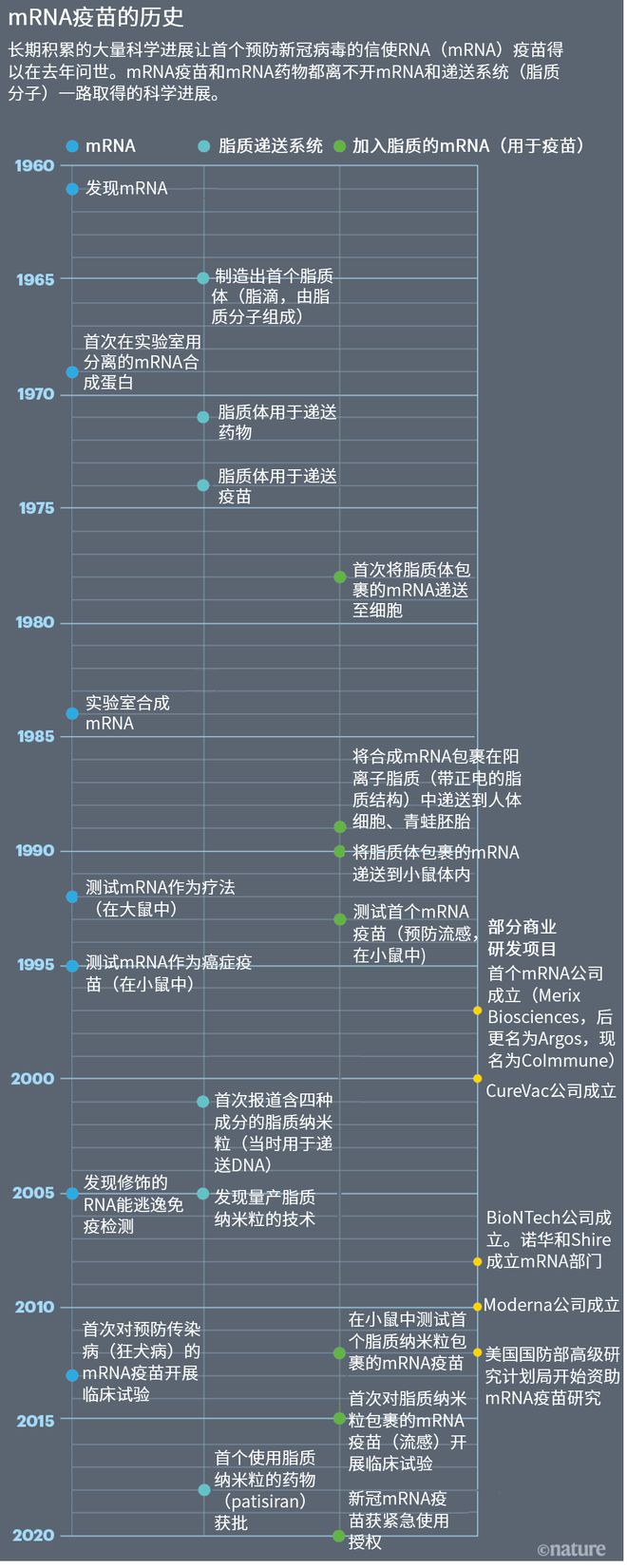
图3mRNA疫苗|图源:Nik Spencer/Nature;改编自U. Şahin et al. Nature Rev. Drug Discov. 13, 759–780 (2014)和X. Hou et al. Nature Rev. Mater. https://doi.org/gmjsn5 (2021).
没想到新冠疫情加快了mRNA疫苗的临床进展,它被逐渐证明是一款高有效率的疫苗工具,成为遏制新冠疫情的重要工具。
此前罗西在媒体采访时表示,卡里科和魏斯曼应该获诺贝尔奖,“如果有一天谁让我推荐诺贝尔奖推荐人选的话,我会推荐他们,因为这是一个将基础科学研究推向临床并挽救了整个世界的故事”。
莫德纳联合创始人Chien也表示,“包括莫德纳内的所有mRNA公司都归功于卡里科和魏斯曼的原创工作。如果没有他们的发现,RNA疫苗将不会像现在这样先进。”
将mRNA保护并送入细胞
加上诺贝尔奖,mRNA技术在过往几年内几乎获得了所在领域所有重要的奖项,但像几乎所有获奖领域一样,科学的突破绝不仅仅是一两个人的功劳。
2021年9月,《自然》(Nature)刊发了一篇长文 “The tangled history of mRNA vaccines”,回顾了mRNA技术的发展历程,从发现mRNA,到人工合成mRNA,到如何修饰mRNA降低免疫反应,再到mRNA递送系统的开发,均有涉及。
作者Elie Dolgin采访了大量的科学家,给我们展现了在mRNA疫苗领域,除了呼声很高的卡里科和魏斯曼,还有一项重要技术——脂质纳米粒(LNP),这种微小脂滴能保护mRNA并将其送入细胞。
这项技术来自皮特·库里斯(Pieter Cullis)的实验室和他创立或管理的多家公司。库里斯是加拿大不列颠哥伦比亚大学的生物化学家。在牛津大学做博士后时,他从物理学转向生物化学,在与同事的合作中,接触到生物膜中脂质的结构性质,从那时起,他被脂质的多态性深深吸引,开启了长达50年的研究。
90年代末起,他的实验室和公司便首创将LNP用于递送能让基因失去活性的核酸链。

图4Pieter Cullis|图源:Paul Joseph for UBC
2012年,库里斯的两家公司开始转型,探索LNP递送系统在基于mRNA的药物中的应用前景。比如温哥华的 Acuitas Therapeutics 公司与魏斯曼在宾大的团队以及多家mRNA公司合作,共同测试mRNA-LNP的不同配比。其中一个配比已经被BioNTech和CureVac的新冠疫苗所使用。Moderna公司的LNP复合物也与此类似。
这种纳米粒含有四种脂质分子:三个分子决定结构和稳定性;第四个名为可电离脂质的分子是LNP有效的关键。这种物质在实验条件下带正电,与Felgner开发的、Malone在80年代末测试的脂质体具有类似优势。但库里斯和商业伙伴开发的可电离脂质能在生理条件下(如在血液中)变成中性,这样能减少对人体的毒性。
无论是修饰mRNA还是LNP,在2020年之前都没有任何一家公司完成了全部临床试验。
面对突如其来的的新冠疫情,莫德纳公司和BioNTech公司倾巢而动。其中,莫德纳与美国国家过敏和传染病研究所(NIAID)合作开展小鼠研究和人体试验,只用了不到10周时间。
2020年3月,BioNTech与纽约制药公司辉瑞(Pfizer)合作,在不到8个月的时间里破纪录地走完了从首次人体试验到紧急使用批准的流程。
虽然mRNA发展史上的有些人认为自己应该得到更多的认可,包括Malone,但其他人却更愿意分享这份荣誉。回顾过去,许多参与者都表示很高兴mRNA疫苗能给人类带来改变,以及自己有幸做出了有价值的贡献。
“所有人都在添砖加瓦,包括我。” 卡里科对《自然》说。


[1]https://mujeresconciencia.com/2021/01/21/katalin-kariko-la-bioquimica-que-entendio-como-utilizar-el-arn-mensajero-para-curarnos-e-inmunizarnos/
[2]https://u-szeged.hu/news-and-events/2021/katalin-kariko-an-alumna
[3]https://www.wired.co.uk/article/mrna-vaccine-revolution-katalin-kariko
[4]https://www.nytimes.com/2021/04/08/health/coronavirus-mrna-kariko.html
[5]https://edition.cnn.com/2020/12/16/us/katalin-kariko-covid-19-vaccine-scientist-trnd/index.html
[6]https://en.wikipedia.org/wiki/Katalin_Karik%C3%B3
[7]Karikó, K., Buckstein, M., Houping, N. & Weissman, D. Immunity 23, 165–175 (2005).
[8]https://www.nature.com/articles/d41586-021-02483-w?utm_source=Wechat&utm_medium=socials&utm_campaign=d41586-021-02483-w